Chez Medistri, nous comprenons que chaque résultat de laboratoire n'est fiable que si la méthode qui le sous-tend l'est également. La validation des méthodes analytiques est le processus par lequel un laboratoire démontre, par des preuves documentées et objectives, qu'une méthode est adaptée à son objectif prévu. Pour les fabricants de dispositifs médicaux, les méthodes validées ne sont pas optionnelles : elles sont une exigence réglementaire dans les cadres ISO/IEC 17025, Bonnes Pratiques de Laboratoire (BPL) et Bonnes Pratiques de Fabrication (BPF). Cet article fournit un aperçu de la manière dont Medistri aborde la validation des méthodes, des paramètres clés que nous évaluons et de l'importance de ce travail pour la sécurité et la conformité de vos produits.
Pourquoi la validation des méthodes est-elle importante ?
Les tests de dispositifs médicaux génèrent des données qui informent directement les décisions réglementaires — des études de caractérisation chimique selon l'ISO 10993-18 à la validation de nettoyage et à l'analyse des résidus. Si la méthode analytique sous-jacente n'a pas été formellement validée, la fiabilité de ces données ne peut pas être démontrée aux régulateurs, aux organismes notifiés ou aux auditeurs.
La validation des méthodes fournit une assurance documentée qu'une méthode analytique produit de manière cohérente des résultats qui sont précis, exacts et reproductibles dans des conditions définies. Elle établit également les limites dans lesquelles une méthode peut être utilisée — la plage de concentration, les types de matrices et les limites en dessous desquelles les résultats ne doivent pas être rapportés à des fins quantitatives.
Cadre réglementaire et normatif
L'approche de validation de Medistri est alignée sur des normes et des documents d'orientation reconnus internationalement :
- ISO/IEC 17025 : La norme internationale pour la compétence des laboratoires d'essai et d'étalonnage. Elle exige que les laboratoires valident les méthodes non standard, les méthodes développées en laboratoire et les méthodes standard utilisées en dehors de leur portée prévue. Dans le cadre d'une accréditation de type C, le laboratoire démontre sa compétence à développer et à valider des méthodes analytiques au sein d'une famille technologique définie.
- Directives de la FDA pour la validation des méthodes chimiques (3e édition, 2019) : Cette directive définit des critères d'acceptation dépendants de la concentration pour la récupération, la répétabilité (RSDr) et la reproductibilité (RSDR), que Medistri applique comme références quantitatives tout au long de ses études de validation.
- BPL (Principes de Bonnes Pratiques de Laboratoire de l'OCDE) : Pour les études soutenant les évaluations de sécurité, les BPL exigent que les méthodes analytiques utilisées soient validées et que tous les changements soient contrôlés et documentés. Les méthodes validées de Medistri peuvent être utilisées pour soutenir des études BPL, à condition que les conditions validées soient respectées et appliquées sans modification ou dans le cadre d'une gestion des changements contrôlée.
- GUM (Guide pour l'expression de l'incertitude de mesure) : Fournit le cadre pour estimer l'incertitude de mesure — un composant obligatoire de toute méthode quantitative validée.
Paramètres clés de validation
Chaque étude de validation chez Medistri suit un plan expérimental structuré. Les paramètres évalués représentent les exigences minimales de validation applicables à toutes les méthodes développées sous une famille technologique donnée. Les paramètres suivants forment le cœur de chaque validation :
Tests de convenance du système (SST)
Avant que des données de validation ne soient générées, le système analytique doit démontrer qu'il fonctionne dans des limites de performance acceptables. Le SST vérifie la performance de l'instrument et de la colonne ainsi que la performance d'intégration spécifique à la méthode dans des conditions de routine. Des critères d'acceptation sont définis pour chaque composant du SST et doivent être remplis avant de procéder à la validation.
Linéarité
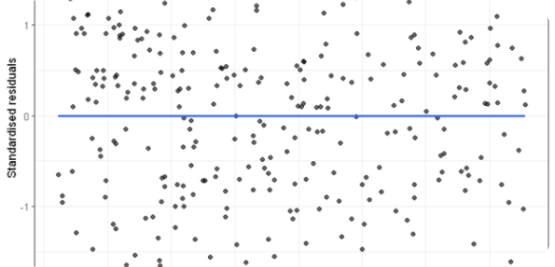
La linéarité est évaluée en analysant des standards de calibration couvrant la plage de concentration prévue sur plusieurs jours, chacun préparé à partir de solutions de travail fraîchement préparées. La fonction de réponse est évaluée par le coefficient de détermination (R² ≥ 0,990), le coefficient de corrélation (R ≥ 0,995) et l'inspection visuelle du graphique des résidus pour confirmer l'absence de courbure systématique.
Limite de détection (LOD) et limite de quantification (LOQ)
La LOD représente la plus faible quantité d'analyte qui peut être détectée de manière fiable, tandis que la LOQ est la plus faible concentration à laquelle une détermination quantitative est réalisée avec une précision et une exactitude appropriées. Chez Medistri, la LOD et la LOQ sont déterminées en utilisant deux approches complémentaires : une méthode de rapport signal/bruit basée sur des mesures de blanc (S/N ≥ 3 pour la LOD, ≥ 10 pour la LOQ), et une approche de confirmation basée sur des mesures répétées à la plus faible concentration standard. Les résultats en dessous de la LOQ établie ne sont pas rapportés à des fins quantitatives.
Répétabilité instrumentale
La répétabilité évalue la proximité des résultats obtenus dans les mêmes conditions d'exploitation — même opérateur, même instrument, même jour. Elle est évaluée en analysant des répliques à plusieurs niveaux de concentration sur plusieurs séries analytiques. L'écart-type relatif (RSD) à chaque niveau doit se situer dans les limites d'acceptation dépendantes de la concentration définies par les directives de la FDA.
Précision intermédiaire
La précision intermédiaire mesure la variabilité des résultats lorsque les conditions sont délibérément modifiées — différents opérateurs, différents jours et différentes préparations de solutions primaires. Le design expérimental implique un minimum de deux opérateurs réalisant plusieurs séries sur différents jours, garantissant une pertinence statistique conformément aux principes de l'ISO 5725. Les valeurs de RSD doivent rester dans les limites de reproductibilité (RSDR) spécifiées par les directives de la FDA pour chaque niveau de concentration.
Exactitude
L'exactitude évalue le degré d'accord entre le résultat mesuré et la valeur réelle. Elle est déterminée en calculant le pourcentage de récupération à tous les niveaux de concentration utilisés dans les études de répétabilité et de précision intermédiaire. Les valeurs de récupération doivent se situer dans les plages d'acceptation dépendantes de la concentration définies par les directives de la FDA — par exemple, 80–110 % de récupération au niveau de 1–10 ppm, avec des plages plus strictes à des concentrations plus élevées.
Stabilité des standards et des solutions
La stabilité des solutions standard dans des conditions de stockage définies est évaluée sur une période reflétant le temps de stockage maximum anticipé dans des conditions de laboratoire de routine. Des aliquotes sont analysées à des intervalles définis, et les résultats sont évalués par rapport à l'incertitude établie de la méthode pour confirmer qu'aucune dégradation significative ne se produit pendant la période de stockage validée.
Incertitude de mesure
L'estimation de l'incertitude de mesure est une exigence obligatoire selon l'ISO/IEC 17025. L'approche de Medistri suit les principes du GUM : identification des sources d'incertitude (préparation standard, exactitude, répétabilité), calcul des incertitudes standards pour chaque source, combinaison de celles-ci et application d'un facteur de couverture (k=2) pour un niveau de confiance de 95 % afin de déterminer l'incertitude élargie. L'incertitude élargie doit rester dans les critères d'acceptation prédéfinis — généralement ≤ 25 % pour la quantification à des niveaux traces.
Comment une étude de validation est conduite chez Medistri
Chaque validation commence par un protocole de validation formel qui définit la portée, la méthode analytique, le plan expérimental et les critères d'acceptation avant que tout travail de laboratoire ne soit initié. Le protocole est examiné et approuvé par le responsable technique, l'ingénierie qualité, le responsable qualité et le responsable de laboratoire.
Le travail expérimental est ensuite réalisé conformément au plan défini : deux opérateurs effectuent des analyses sur plusieurs séries à différents jours en utilisant des solutions fraîchement préparées. Tout l'équipement critique est calibré et qualifié avant utilisation, et la préparation des échantillons et l'analyse instrumentale sont effectuées dans des zones de laboratoire désignées et identifiées pour minimiser le risque de contamination croisée — conformément aux exigences des SOP internes et aux principes des BPL.
Les résultats sont compilés dans un rapport de validation de méthode, qui documente toutes les données expérimentales, les évaluations statistiques, les conclusions pour chaque paramètre et toute déviation ou résultat hors spécification. Le rapport comprend un tableau récapitulatif présentant le résultat de chaque test de validation par rapport à ses critères d'acceptation, et se conclut par une déclaration formelle de conformité.
Assurer la conformité aux BPL
Le cadre de validation de Medistri est conçu pour soutenir à la fois les tests accrédités selon l'ISO/IEC 17025 et les études réglementées par les BPL. Plusieurs éléments du processus de validation répondent directement aux exigences des BPL :
- Des zones de test identifiées et dédiées sont utilisées pour les différentes étapes de l'étude — préparation des échantillons dans une zone de préparation désignée, et analyses instrumentales dans une zone analytique dédiée — garantissant un contrôle environnemental approprié.
- L'Unité d'Assurance Qualité opère indépendamment de la conduite de l'étude et peut auditer la documentation de validation pour confirmer sa pertinence pour le soutien des études BPL.
- Tous les changements apportés aux méthodes validées sont classés comme mineurs ou majeurs en fonction de leur impact potentiel sur la performance analytique. Les changements mineurs (tels que des consommables équivalents ou le remplacement de colonnes avec des spécifications identiques) sont justifiés et documentés. Les changements majeurs (tels qu'un changement de principe analytique ou de stratégie de calibration) nécessitent une évaluation préalable et peuvent déclencher une revalidation partielle ou complète.
- Pour les études BPL spécifiquement, tous les changements doivent être approuvés avant leur mise en œuvre et documentés conformément aux exigences des BPL.
Vérification continue des méthodes par le biais de tests de compétence
La validation n'est pas un événement unique. Une fois qu'une méthode est validée et mise en routine, sa performance continue doit être surveillée. Medistri participe à des programmes de tests de compétence (PTS) et à des comparaisons interlaboratoires (ILC) pour vérifier en continu la compétence de ses méthodes d'essai accréditées.
Les fournisseurs de tests de compétence utilisés par Medistri sont accrédités selon l'ISO/IEC 17043. Les résultats sont évalués à l'aide de scores z calculés conformément à l'ISO 13528 : un score z de |z| ≤ 2,00 est considéré comme satisfaisant, des valeurs entre 2,00 et 3,00 sont douteuses, et |z| ≥ 3,00 est insatisfaisant. Chaque résultat de test de compétence est vérifié en interne et documenté dans un rapport de conformité signé par le personnel technique responsable et le département qualité.
Pourquoi cela compte pour vos produits
Pour les fabricants de dispositifs médicaux, travailler avec un laboratoire qui suit une approche de validation rigoureuse et documentée signifie que les données analytiques soutenant vos soumissions réglementaires sont défendables et traçables. Que les données soient utilisées pour la caractérisation chimique selon l'ISO 10993-18, la validation de nettoyage, les tests de solvants résiduels ou l'analyse des extractibles et des lixiviables, la méthode sous-jacente doit être validée selon les normes attendues par les autorités réglementaires et les organismes notifiés.
Le cadre de validation de Medistri — aligné sur l'ISO/IEC 17025, les directives de la FDA, les principes des BPL et le GUM — fournit la base scientifique dont les fabricants ont besoin pour soutenir la sécurité des produits et la conformité réglementaire tout au long du cycle de vie du dispositif.
En savoir plus sur notre laboratoire ici. Pour garantir que vos produits répondent aux normes de qualité et de sécurité les plus élevées, contactez notre équipe dédiée à contact@medistri.com.
— L'équipe Medistri
#Medistri
Medistri est la principale entreprise indépendante de stérilisation sous contrat en Europe, fondée en 2006 et ayant son siège au cœur de la Suisse. Nous sommes un acteur mondial fournissant une infrastructure essentielle qui alimente l'innovation en matière de santé dans le monde entier.
Nous servons des clients de toutes tailles, des startups, des projets universitaires et des instituts de recherche aux entreprises du Fortune 500, dans les domaines des dispositifs médicaux, de l'emballage pharmaceutique et de la biotechnologie.
Medistri soutient des produits à chaque étape du cycle de vie : développement préclinique, mise sur le marché et industrialisation complète.
Notre solution intégrée, de bout en bout, permet à nos clients de se concentrer sur ce qui compte le plus : ingénierie, innovation et développement, tandis que nous gérons les processus critiques en arrière-plan.
Nos départements synchronisés travaillent ensemble pour fournir un ensemble complet de services :
- Services de stérilisation et de validation sous contrat
- Services de laboratoire sous contrat
- Services de fabrication sous contrat
- Services logistiques
- Services de conseil
Nous vous aidons à accélérer le temps de mise sur le marché, à réduire les barrières à l'échelle et à fournir des solutions de santé plus sûres et plus durables aux patients du monde entier.
Solutions de Medistri pour les produits en phase préclinique
Au cours de la phase préclinique, l'exécution est essentielle pour valider les concepts, générer des données fiables et établir une base solide pour l'approbation réglementaire.
Medistri sert de partenaire d'infrastructure intégré, offrant un portefeuille complet de solutions internes optimisées pour la R&D et le développement de preuves de concept.
Nos solutions englobent des cycles de traitement R&D (protocoles de stérilisation personnalisés), nettoyage et reprocessing, assemblage de produits et emballage, ainsi que des tests spécialisés, y compris la biocompatibilité, les extractibles et les lixiviables, l'intégrité de la barrière stérile, le conditionnement environnemental, le développement d'analyses de laboratoire, la libération de lots et le conseil réglementaire.
Ce modèle verticalement intégré minimise la coordination des fournisseurs, accélère les itérations de développement, garantit l'intégrité des données et la conformité dès le départ, et permet à votre équipe de prioriser les avancées scientifiques et techniques essentielles.
Vous positionnant pour une progression sans heurts vers les essais cliniques et la commercialisation.
Foire aux questions
1. Qu’est-ce que la validation d’une méthode analytique dans le cadre des essais de dispositifs médicaux ?
La validation d’une méthode analytique consiste à démontrer qu’une méthode de laboratoire est adaptée à l’usage prévu. Elle fournit des preuves objectives que la méthode produit des résultats exacts, précis et reproductibles dans des conditions définies.
2. Pourquoi la validation des méthodes est-elle requise pour la conformité réglementaire ?
Les cadres réglementaires tels que l’ISO/CEI 17025, les BPL et les BPF exigent des méthodes validées afin de garantir la fiabilité des données. Sans validation, les résultats d’essai ne peuvent pas être considérés comme scientifiquement justifiés ni acceptables lors d’audits, d’inspections ou de soumissions réglementaires.
3. Comment les méthodes analytiques sont-elles validées en pratique ?
La validation consiste à évaluer des paramètres clés tels que la linéarité, l’exactitude, la précision, les limites de détection et de quantification, ainsi que l’incertitude de mesure. Ces paramètres définissent les performances de la méthode et les conditions dans lesquelles les résultats peuvent être interprétés de manière fiable.
4. Quand une méthode analytique doit-elle être validée ou revalidée ?
Une méthode doit être validée avant son utilisation en routine et revalidée en cas de modifications significatives, comme un changement de technique analytique, d’équipement ou de stratégie d’étalonnage. Une vérification continue est également nécessaire pour garantir la performance dans le temps.
5. Comment Medistri garantit-elle la fiabilité de la validation des méthodes analytiques ?
Medistri applique un cadre de validation structuré conforme à l’ISO/CEI 17025, aux recommandations de la FDA, aux principes des BPL et au GUM. En combinant des pratiques de laboratoire maîtrisées, des évaluations statistiques et un suivi continu des performances, Medistri assure la production de données robustes et traçables pour les exigences réglementaires.