NEW
Strategien zur Validierung der Sterilisation für Hersteller von Medizinprodukten
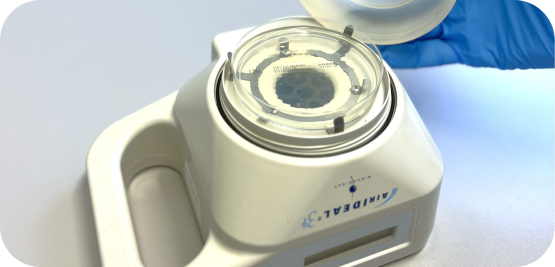
Für medizinische Geräte und pharmazeutische Produkte, die als steril vermarktet werden, stellt die Validierung der Sterilisation einen kritischen Übergangspunkt zwischen Entwicklung und routinemäßiger kommerzieller Herstellung dar. In diesem Stadium müssen Hersteller nachweisen, dass das endgültige Produkt, das Verpackungssystem und die Herstellungs-Konfiguration unter kontrollierten und reproduzierbaren Bedingungen sterilisiert werden können, während die Produktleistung und die Einhaltung der regulatorischen Anforderungen gewährleistet bleiben.
NEW
Medistri offiziell im Schweizer GLP-Überwachungsprogramm gelistet
Medistri freut sich bekannt zu geben, dass unser Labor nun offiziell im Schweizer GLP-Überwachungsprogramm unter der Aufsicht der Schweizer Bundesbehörden und Swissmedic gelistet ist.
NEW
Umweltüberwachung für Hersteller von Medizinprodukten
Medizinprodukte werden in Umgebungen hergestellt, montiert und verpackt, in denen Kontaminationen, sei es partikulär, mikrobiologisch oder chemisch, die Produktsicherheit direkt gefährden können. Die Umweltüberwachung ist der systematische Prozess zur Messung und Dokumentation der Bedingungen in diesen Umgebungen, der den Herstellern die Beweise liefert, die sie benötigen, um nachzuweisen, dass ihre Produktionsbereiche unter Kontrolle sind.
Nachvalidierungstraining
Die Sterilisationsvalidierung endet nicht mit der Zyklusfreigabe. Da sich die regulatorischen Anforderungen weiterentwickeln, erfordern die Aufrechterhaltung validierter Bedingungen, die Steuerung von Änderungen und die Sicherstellung einer konsistenten Routinefreigabe eine strukturierte Expertise innerhalb der internen Teams.
NEW
Ein Überblick über die "Großen Drei": Zytotoxizität, Reizung und Sensibilisierungstests
Für nahezu alle medizinischen Geräte bilden drei biologische Endpunkte die Grundlage einer biologischen Sicherheitsbewertung gemäß ISO 10993-1: Zytotoxizität, Reizung und Sensibilisierung. Diese häufig als die "Großen Drei" bezeichneten Endpunkte sind auf praktisch alle Gerätekategorien anwendbar, unabhängig von der Art oder Dauer des Patientenkontakts. Bei Medistri werden Hersteller in diesen drei Endpunkten durch eine Kombination aus internen In-vitro-Tests und koordinierten In-vivo-Studien unterstützt, um sicherzustellen, dass die biologische Sicherheit mit wissenschaftlicher Strenge nachgewiesen wird und den regulatorischen Erwartungen entspricht.
Wiederaufbereitung und Reinigungsvalidierung für Medizinprodukte
In der Herstellung von Gesundheitsprodukten und klinischen Umgebungen ist die Kontaminationskontrolle eine grundlegende regulatorische und patientensicherheitsrelevante Verpflichtung. Medizinprodukte können biologischen Kontaminanten durch klinische Nutzung oder chemischen und partikulären Rückständen, die während der Herstellung entstehen, ausgesetzt sein. Sowohl die Validierung der Wiederaufbereitung als auch die Reinigungsvalidierung sind daher erforderliche Disziplinen, die jeweils durch unterschiedliche regulatorische Rahmenbedingungen geregelt sind, jedoch ein gemeinsames Ziel verfolgen: nachzuweisen, dass Kontaminationen effektiv und reproduzierbar auf ein Niveau reduziert werden, das die Sicherheit, Funktionalität oder beabsichtigte Leistung des Geräts nicht gefährdet.
NEW
Prozesskontrolle, Rückverfolgbarkeit und Industrialisierung in der Montage von Gesundheitsprodukten
Gesundheitsprodukte werden selten als isolierte Komponenten an Krankenhäuser geliefert. Stattdessen werden sie zunehmend als vorkonfigurierte Verfahrenskits bereitgestellt, die mehrere sterile oder nicht-sterile Komponenten enthalten, die für einen bestimmten klinischen Eingriff erforderlich sind. Diese Kits können Implantate, Einweggeräte, Arzneimittel, Zubehör und Schutzmaterialien umfassen, die in einem einzigen validierten Verpackungssystem zusammengefasst sind.
NEW
Individuelle Zyklusentwicklung
Sterilisationsprozesse sind oft mit standardisierten Zyklusrezepten verbunden, die darauf ausgelegt sind, eine breite Palette von Gesundheitsprodukten zu behandeln. In der Praxis erfordern jedoch viele medizinische Geräte, pharmazeutische Komponenten und Verpackungssysteme Sterilisationsbedingungen, die nicht zuverlässig mit vordefinierten Zyklusparametern angesprochen werden können.
NEW
ISO 10993-1:2025 — Auswirkungen auf chemische Charakterisierung und E&L-Programme
Bei Medistri arbeiten wir seit der Veröffentlichung im November gemeinsam mit unseren Kunden an der Umsetzung der Revision 2025 der ISO 10993-1. Die häufigste Frage lautet dabei: Müssen wir unsere bestehende chemische Charakterisierung und toxikologische Risikobewertung neu durchführen? Die ehrliche Antwort lautet: Es kommt darauf an — und häufiger als viele Hersteller erwarten, lautet die Antwort nein oder noch nicht. In den meisten Fällen betrifft die notwendige Anpassung vor allem die Art und Weise, wie vorhandene Arbeiten dokumentiert und innerhalb der biologischen Bewertungsakte strukturiert werden. Dieser Artikel erläutert, wo die tatsächlichen Unterschiede liegen.
NEW
Medistri wird Mitglied von Swiss Medtech
Medistri freut sich, seine offizielle Mitgliedschaft bei Swiss Medtech bekannt zu geben, dem führenden Verband der Schweizer MedTech-Industrie. Diese Mitgliedschaft stellt einen wichtigen Schritt dar, um Medistris aktive Beteiligung innerhalb des Schweizer Gesundheits- und MedTech-Ökosystems weiter zu stärken.
Seitennummerierung
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- …
- Nächste Seite
- Letzte Seite